Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
柏木 啓次; 及川 将一*; 島田 博文*; 百合 庸介; 上松 敬; 石井 保行; 齋藤 勇一; 酒井 卓郎; 奥村 進; 倉島 俊; et al.
no journal, ,
加齢黄班変性症,脳下垂体腫瘍,動脈瘤の治療部位の大きさはそれぞれ1 1mm, 30
1mm, 30 30mm, 3mm
30mm, 3mm 3mmである。これらを手術することなく切らずに重粒子線によって治療するためには、ビームスポット径が100マイクロメートルでビーム径が深度にほとんど依存しないペンシルビームの形成が必要である。本研究では、21世紀COEプログラムの一環として、このペンシルビームを患部に3次元的にスポットスキャニングするための最適なビーム輸送システムについてビーム光学的検討に基づく設計を行った。なお、この設計においては、群馬大学に建設予定の粒子線治療施設のビーム輸送ラインをモデルとした。ビーム光学計算コードにより偏向電磁石及び四重極電磁石等で構成される光学系に関して、目的のビームを得るためにそれらのパラメータの最適化を行った。次に、拡大ブラッグピークを得るためのレンジシフターの挿入によるビームの散乱効果(エミッタンスの増大)を評価した。本報告では、システムの全体構成とビーム光学計算について、ポスターにして詳細に解説する。
3mmである。これらを手術することなく切らずに重粒子線によって治療するためには、ビームスポット径が100マイクロメートルでビーム径が深度にほとんど依存しないペンシルビームの形成が必要である。本研究では、21世紀COEプログラムの一環として、このペンシルビームを患部に3次元的にスポットスキャニングするための最適なビーム輸送システムについてビーム光学的検討に基づく設計を行った。なお、この設計においては、群馬大学に建設予定の粒子線治療施設のビーム輸送ラインをモデルとした。ビーム光学計算コードにより偏向電磁石及び四重極電磁石等で構成される光学系に関して、目的のビームを得るためにそれらのパラメータの最適化を行った。次に、拡大ブラッグピークを得るためのレンジシフターの挿入によるビームの散乱効果(エミッタンスの増大)を評価した。本報告では、システムの全体構成とビーム光学計算について、ポスターにして詳細に解説する。
 1 on HUVEC
1 on HUVEC清原 浩樹*; 石崎 泰樹*; 鈴木 義行*; 浜田 信行*; 舟山 知夫; 和田 成一*; 坂下 哲哉; 小林 泰彦; 中野 隆史*
no journal, ,
放射線誘発損傷/線維症の領域で炎症性細胞接着とサイトカインの増加が観察されている。われわれは、正常ヒト臍帯静脈内皮細胞HUVECにおいて、細胞接着分子ICAM-1と増殖因子TGF- 1の発現における重イオンビーム照射効果について研究した。HUVECの培養細胞に炭素イオンビーム0.1-0.5Gyを一度に照射した。照射後24時間又は48時間後に細胞を固定し、抗ICAM-1抗体とFITC接合二次抗体で標識した。照射によるICAM-1発現の増加がTGF-
1の発現における重イオンビーム照射効果について研究した。HUVECの培養細胞に炭素イオンビーム0.1-0.5Gyを一度に照射した。照射後24時間又は48時間後に細胞を固定し、抗ICAM-1抗体とFITC接合二次抗体で標識した。照射によるICAM-1発現の増加がTGF- 1発現の抑制によって変わるかどうかを調べるために、照射の2時間にTGF-
1発現の抑制によって変わるかどうかを調べるために、照射の2時間にTGF- 1受容体キナーゼ阻害剤SB431542を添加した。HUVECにおけるICAM-1の発現は、炭素イオンビーム照射によって増加したが、線量や固定時間による違いは著しくなかった。照射後にSB431542で処理したグループとコントロールの差もあまりなかった。X線を用いて行った同様の実験の結果も示す。ICAM-1は重イオン照射に対する上皮細胞の応答に関係するが、TGF-
1受容体キナーゼ阻害剤SB431542を添加した。HUVECにおけるICAM-1の発現は、炭素イオンビーム照射によって増加したが、線量や固定時間による違いは著しくなかった。照射後にSB431542で処理したグループとコントロールの差もあまりなかった。X線を用いて行った同様の実験の結果も示す。ICAM-1は重イオン照射に対する上皮細胞の応答に関係するが、TGF- 1と重イオン照射誘発線維症との相関の解明にはさらなる研究が必要である。
1と重イオン照射誘発線維症との相関の解明にはさらなる研究が必要である。
原田 耕作*; 野中 哲生*; 浜田 信行*; 舟山 知夫; 桜井 英幸*; 和田 成一*; 坂下 哲哉; 長谷川 正俊*; 小林 泰彦; 中野 隆史*
no journal, ,
重イオン放射線治療は、優れた線量分布と高い生物学的効果ゆえに、期待されている。しかし、ブロードビームによる細胞死メカニズムは、十分に解明されていない。本研究では、バイスタンダー効果に焦点を当て、p53ヒト肺癌細胞株A549を用い、重イオン照射による細胞死メカニズムを明らかにする。群馬大学のMBR-1505と、TIARA(JAEA)の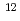 C(220MeV)と
C(220MeV)と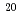 Ne(260MeV)を用い、コンフルエントな細胞にX線を照射し、コロニー形成法で細胞生存率を調べた。X線(150kV),
Ne(260MeV)を用い、コンフルエントな細胞にX線を照射し、コロニー形成法で細胞生存率を調べた。X線(150kV), 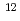 C,
C, 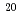 Neを照射した細胞のD
Neを照射した細胞のD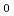 /D
/D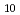 は、それぞれ1.59Gy/4.00Gy, 1.23Gy/2.39Gy, 1.81Gy/4.55Gyだった。細胞50万個中わずか5
は、それぞれ1.59Gy/4.00Gy, 1.23Gy/2.39Gy, 1.81Gy/4.55Gyだった。細胞50万個中わずか5 25個の細胞に100個のイオンを照射することで、非照射対照群と比較して生存率が23
25個の細胞に100個のイオンを照射することで、非照射対照群と比較して生存率が23 48%減少した。バイスタンダー効果は、重イオン照射による細胞死メカニズムに重要な役割を果たしていることがわかった。さらに、DNA修復の細胞応答や重イオン照射によるアポトーシスの研究を進め、臨床分野での重イオン放射線治療法を確立する。
48%減少した。バイスタンダー効果は、重イオン照射による細胞死メカニズムに重要な役割を果たしていることがわかった。さらに、DNA修復の細胞応答や重イオン照射によるアポトーシスの研究を進め、臨床分野での重イオン放射線治療法を確立する。
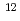 C ion-beam in a glioma cell line latently infected with HTLV-I
C ion-beam in a glioma cell line latently infected with HTLV-I田中 淳*; 大上 厚志*; 清水 宣明*; 和田 成一*; 小林 泰彦; 星野 洪郎*
no journal, ,
UV, X線及び熱中性子は、マウス内在性C型レトロウイルスを誘発するが、ヒト内在性レトロウイルスの誘導は報告されていない。われわれは、標的細胞としてヒトT細胞白血病ウイルスI型(HTLV-I)に感染させたヒト神経膠腫細胞クローンを用い、ヒト細胞の重イオン照射による内在性又は潜伏感染したヒトレトロウイルスの誘導について調べた。HTLV-Iは、成人T細胞性白血病の原因レトロウイルスであり、脊椎障害/熱帯性痙性不全対麻痺症に関連している。HTLV-Iは感染した後、潜伏状態に入る。このとき、HTLV-IのmRNAの発現レベルは低いので、抗原は間接免疫蛍光抗体法(IFA)の検出レベル以下である。HTLV-Iに潜伏感染したヒト神経膠腫細胞クローンに、さまざまな線量の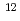 Cイオンビームを照射した。照射5日後にmRNAと抗原の発現を調べた。抗原の発現はIFAによって調べた。
Cイオンビームを照射した。照射5日後にmRNAと抗原の発現を調べた。抗原の発現はIFAによって調べた。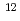 Cイオンビーム照射の結果、全体のmRNA発現に変化はなかったが、抗原の発現が増加したことがIFAによって検出された。重イオンビーム照射は、潜伏感染したヒトレトロウイルスの誘導を導くことがわかった。
Cイオンビーム照射の結果、全体のmRNA発現に変化はなかったが、抗原の発現が増加したことがIFAによって検出された。重イオンビーム照射は、潜伏感染したヒトレトロウイルスの誘導を導くことがわかった。
清水 宣明*; 大上 厚志*; 大槻 貴博*; 森 隆久*; 山口 華代*; 中村 孝子*; 和田 成一*; 小林 泰彦; 星野 洪郎*
no journal, ,
受容体CD4や補助受容体CCR5, CXCR4を介したヒト免疫不全ウイルス1型(HIV-1)の細胞侵入機構はまだ十分に解明されていない。われわれは重イオン照射を用いHIV-1感染機構を解明する。C8166/CCR5とNP-2/CD4/CCR5に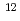 Cイオンビーム, UV, X線を照射した。CCR5, CD4, CXCR4の発現を流動細胞計測法で検出した。両細胞へのHIV-1の感染性を間接免疫蛍光抗体法(IFA)やウエスタンブロットで検出した。細胞増殖や形態変化を顕微鏡で観察した。CCR5, CD4, CXCR4の発現レベルは
Cイオンビーム, UV, X線を照射した。CCR5, CD4, CXCR4の発現を流動細胞計測法で検出した。両細胞へのHIV-1の感染性を間接免疫蛍光抗体法(IFA)やウエスタンブロットで検出した。細胞増殖や形態変化を顕微鏡で観察した。CCR5, CD4, CXCR4の発現レベルは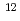 Cイオン, UV, X線に著しい影響を受けた。
Cイオン, UV, X線に著しい影響を受けた。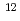 Cイオン照射は細胞増殖を強く抑制し、巨細胞形成を促した。C8166/CCR5とNP-2/CD/CCR5へのHIV-1の感染性は、
Cイオン照射は細胞増殖を強く抑制し、巨細胞形成を促した。C8166/CCR5とNP-2/CD/CCR5へのHIV-1の感染性は、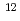 Cイオン照射では数倍に増加したが、UVとX線では変化が弱かった。重イオン照射はCD4とCCR5が介するHIV-1感染過程を促す。重イオン照射により誘導される現象は、HIV-1侵入機構に関与すると考えられ、重イオン照射はHIV-1の侵入にかかわる新規な因子を同定する有用な手段になると期待できる。
Cイオン照射では数倍に増加したが、UVとX線では変化が弱かった。重イオン照射はCD4とCCR5が介するHIV-1感染過程を促す。重イオン照射により誘導される現象は、HIV-1侵入機構に関与すると考えられ、重イオン照射はHIV-1の侵入にかかわる新規な因子を同定する有用な手段になると期待できる。